磺酰胺类分子的研究背景
当前癌症治疗主要面临着耐药性和药物脱靶毒性两大主要挑战,而磺酰胺类化合物结构多样、药效广泛,有望成为更高效低毒的抗癌分子。磺酰胺类分子作为靶向药物和农药的主要活性成分,常被用作羧酸基团的有效生物等排体,能够避免羧酸基团的代谢不稳定性、跨膜扩散受限和毒性等问题。目前部分化合物已被开发为HDAC抑制剂以及拓扑异构酶II抑制剂等上市药物,在抗菌、抗癫痫以及抗肿瘤等领域中被广泛应用。
磺酰胺类衍生物一:芳香化酶抑制剂
乳腺癌作为全球女性中较为严重的恶性肿瘤之一,与体内雌激素浓度过高密切相关。而芳香化酶(Aromatase, 又称 CYP19)负责将雄激素催化转化为雌激素,在雌激素生物合成中发挥核心作用,因此,通过抑制芳香化酶来降低雌激素水平已成为治疗乳腺癌的有效策略。然而,尽管芳香化酶抑制剂展现出良好的临床疗效,但在长期使用过程中仍面临获得性耐药和一些副作用,近年来,基于磺酰胺基团优良的药物构效特性,研究者开发了多种基于磺酰胺的芳香化酶抑制剂。
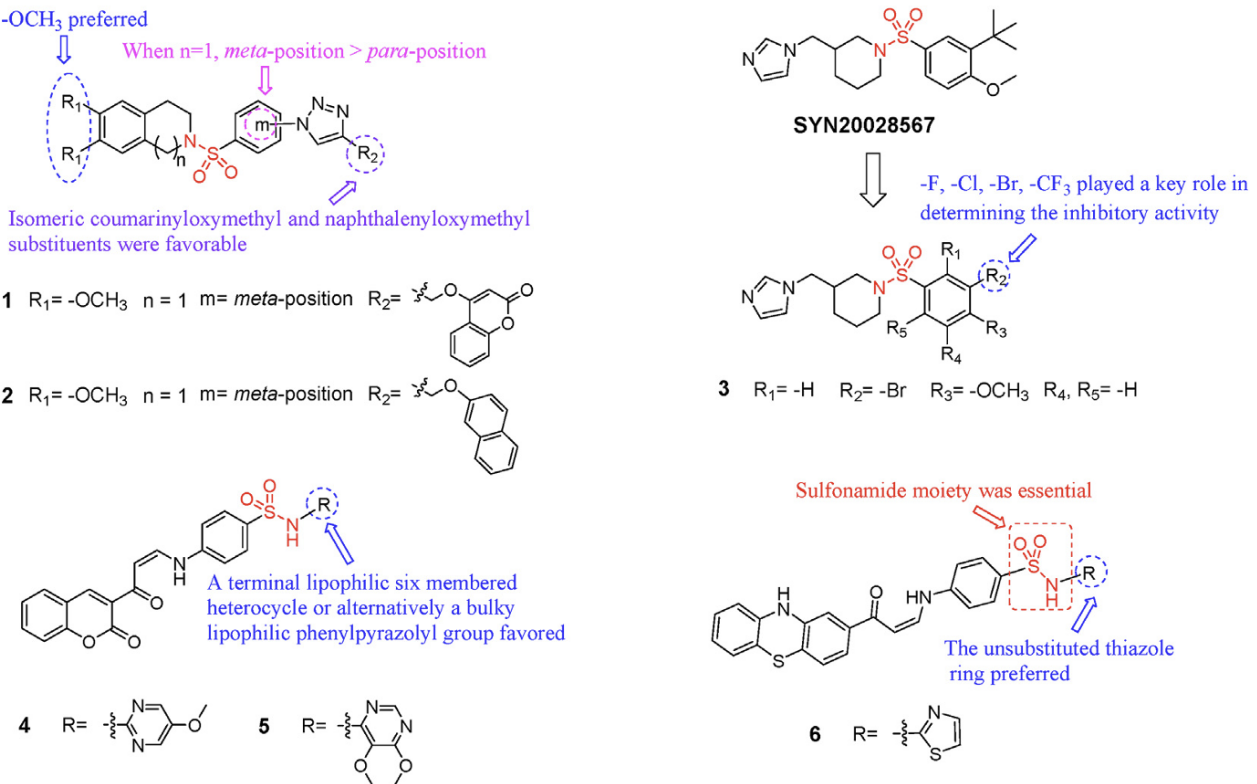
图1 部分基于磺酰胺的芳香化酶抑制剂
Di Matteo 等人通过以已知的先导化合物SYN20028567为基础,设计并合成了一系列基于咪唑基哌啶结构的磺酰胺衍生物,通过半自动化高通量筛选(HTS)进行抑制活性评估,发现化合物3最具活性。此外,在 Pingaew 等人发现的构效关系基础上,Ghorab 等人又开发出一类含有色原烯(chromene)骨架的磺酰胺衍生物作为芳香化酶抑制剂,通过T47D 乳腺癌细胞系评估其抗增殖活性,发现这类化合物均表现出良好的芳香化酶抑制活性,其中化合物 4 和 5 表现最优。进一步的SAR 分析表明,在末端引入疏水性六元杂环或体积较大的苯基吡唑基团,有助于提高芳香化酶抑制活性和乳腺癌细胞的抗增殖作用。
肿瘤微环境中的低氧特征在癌症的发生和发展中起着关键作用,癌细胞能通过降低胞内pH值并改变基因表达方式以适应对正常细胞不利的环境。其中,碳酸酐酶(CA)作为一类锌金属酶,能够通过催化二氧化碳与水的可逆转化反应来调节细胞内外的pH值。其中,CA IX和CA XII在多种肿瘤中表达上调,能促进肿瘤的生长、增殖、侵袭、转移,并使肿瘤细胞获得对放化疗的耐受性,因此被认为是重要的抗癌靶点,近年来已有大量以磺酰胺类结构为核心的抑制剂被开发出来。
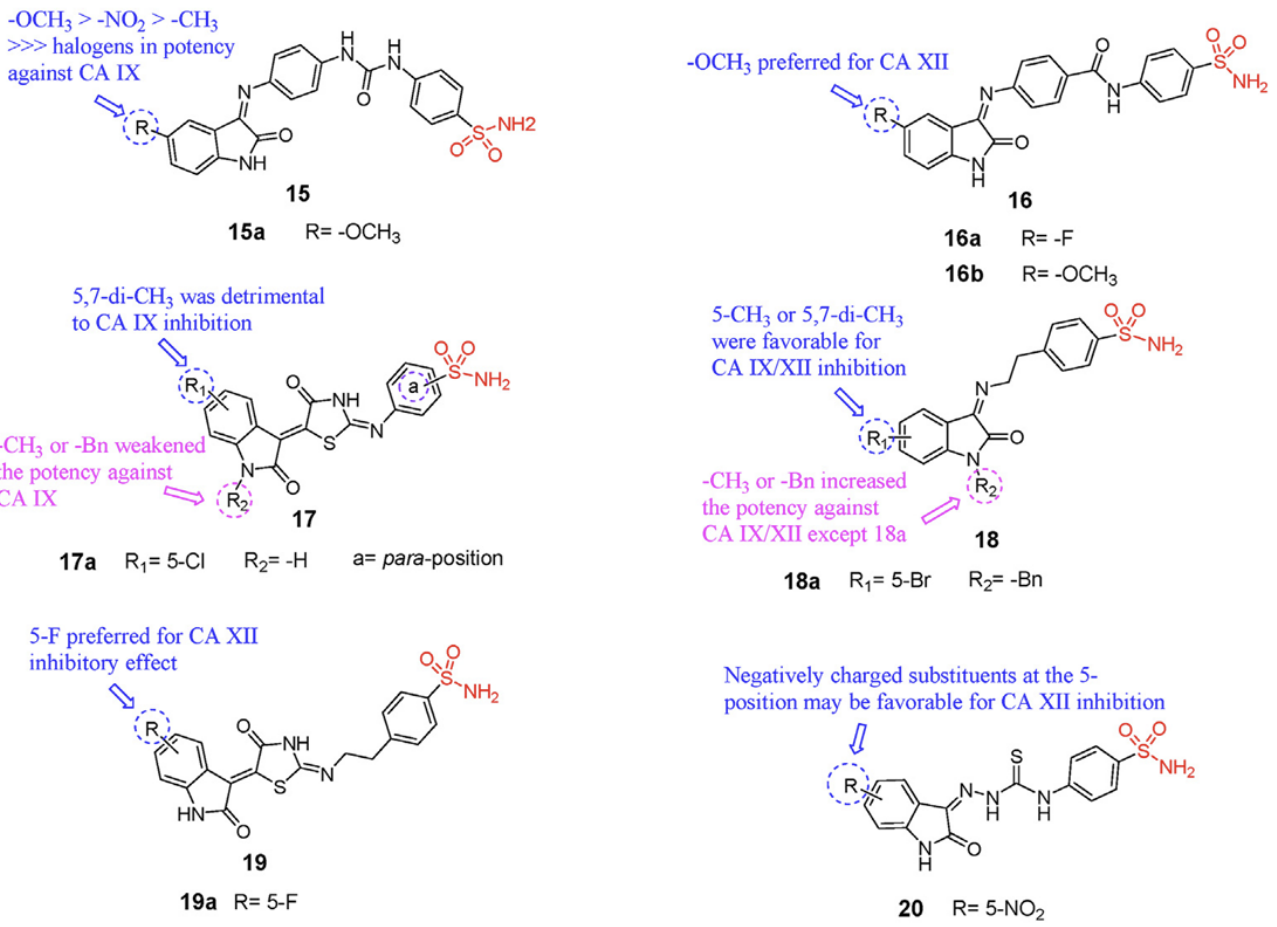
图2 基于磺酰胺的碳酸酐酶抑制剂
Eldehna等人采用分子杂交策略设计合成了两类带有异吲哚酮基团的苯磺酰胺衍生物(图2化合物15和16),经过抑制活性测试,15a和16a分别是两个系列中对CA IX抑制效果最强的化合物。随后,该团队进一步合成了一系列含有异吲哚酮-噻唑烷酮结构的磺酰胺类化合物(图2化合物17),其对CA II和CA IX表现出更优的抑制效果。
杂芳基磺酰胺类的合成路径与优化
传统药物合成方法通常依赖杂芳基磺酰氯与胺制备磺酰胺(图 3A),但这种试剂并不稳定且具有毒性,不适合大规模的工业化操作。随后,一锅法合成策略(图 3B)以及基于铜催化的芳基硼酸和DABSO(硫代二亚磺酸盐)的方法被陆续提出,更有后来电化学氧化偶联法的发展(图 3C),这些方法为磺酰胺的合成提供了无毒替代路线。然而,尽管磺酰胺的合成技术已有显著进步,多杂原子杂芳基磺酰胺的合成仍是难题,需要更高效、温和且安全的策略。
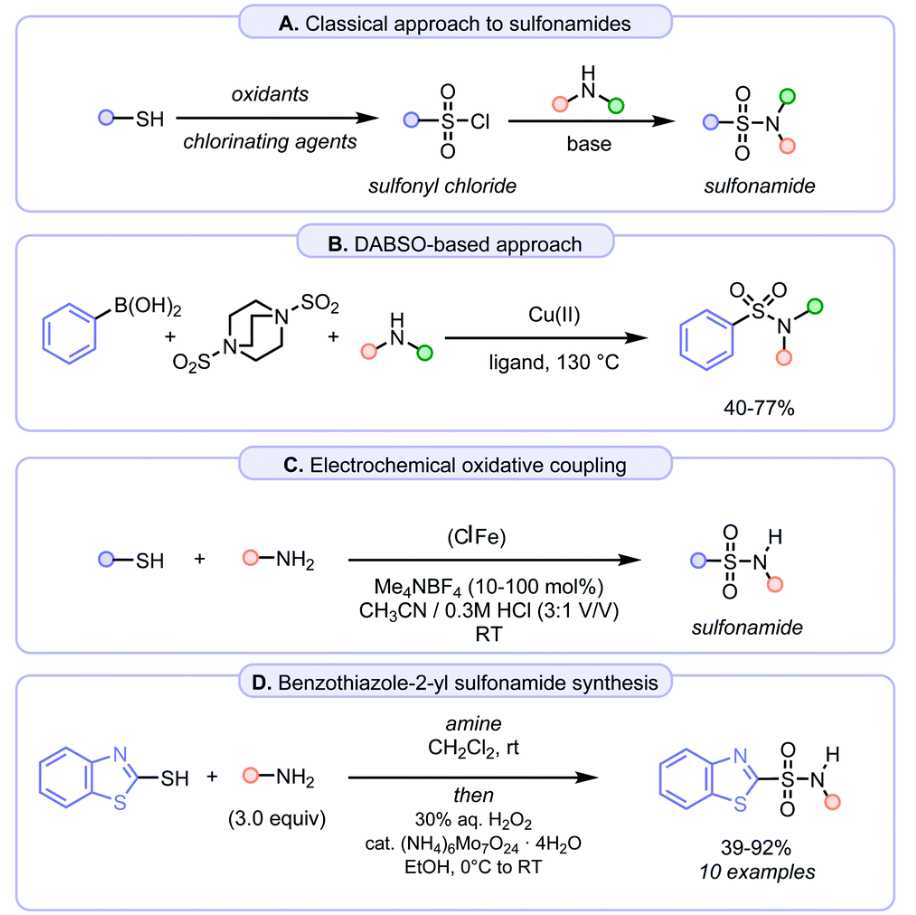
图3 以往的磺酰胺类药物合成路线
N,N-二取代芳杂基磺酰胺合成新方法
氧化偶联合成法利用杂芳基硫醇和伯胺得到N-单取代磺酰胺,解决了 N-取代杂芳基磺酰胺的“初步构建难题”。然而进一步的取代却仍待探索。近年来,捷克科学院、帕拉茨基大学的Roman O. Iakovenko团队提出了微波促进的Fukuyama–Mitsunobu烷基化法,用于进一步合成N,N-二取代的苯并噻唑-2-基磺酰胺,尤其是结构不稳定的苯并恶唑磺酰胺,且产物且兼容立体选择性,保留光学纯度。该方法首先用烷基封住N-单取代磺酰胺上酸性较高的N-H,避免其结构受到周围环境影响而降解。
反应条件稍作修改后,成功转化为 (+)-17f,产率 48%,产物稳定 3个月。合成过程中用到的起始原料苯并噻唑-2-硫醇和烷基胺(alkyl amines),均为易得的大宗化学品,流程简单高效,条件温和,能够高效构建多种类型的杂芳基磺酰胺结构单元,预期将进一步推动其在药物化学等相关领域的开发与应用。
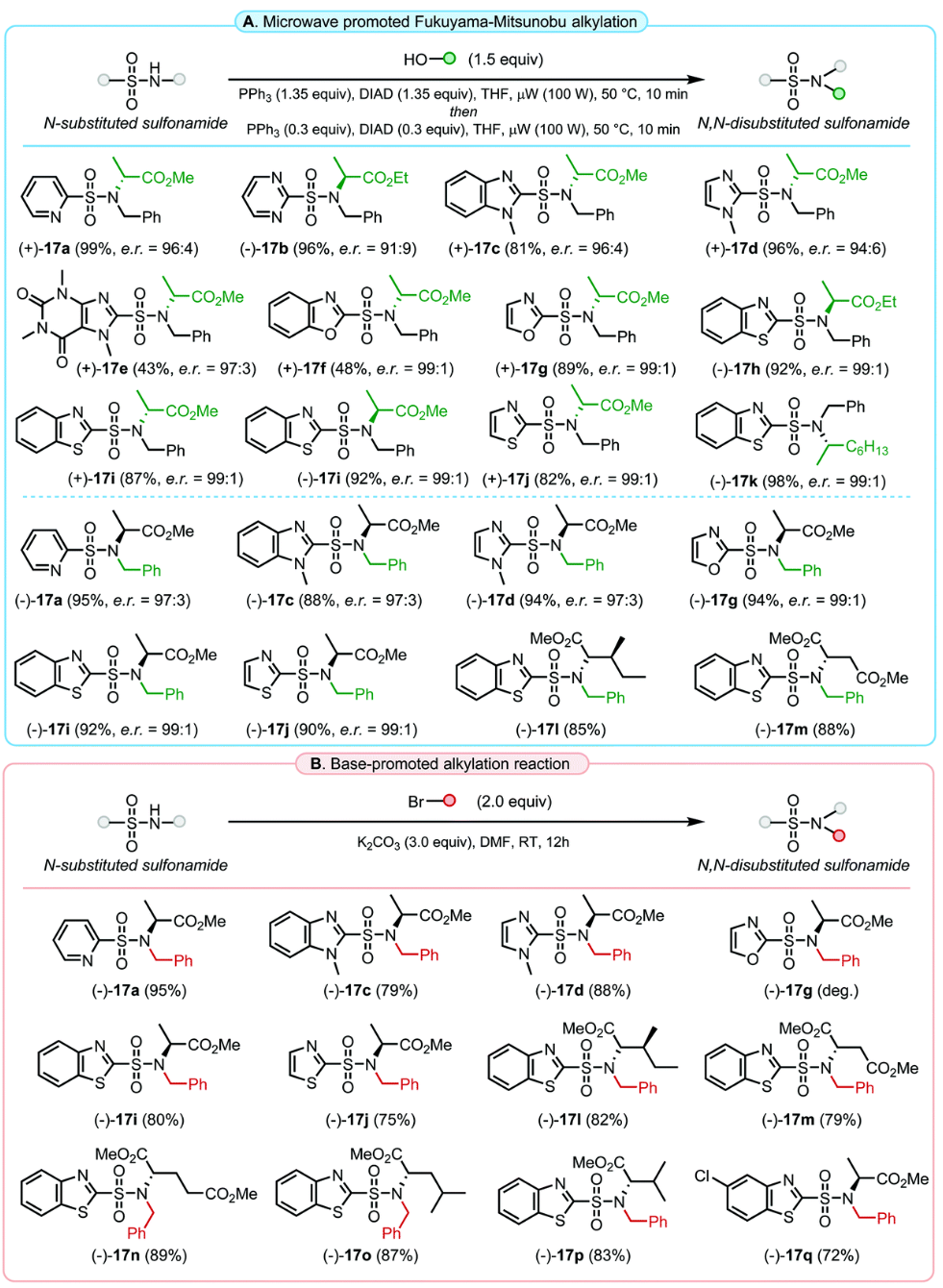
图4 N,N-二取代磺酰胺的合成
相关产品推荐
参考文献
1. 10.1021/acs.jnatprod.7b00921IF: 3.6 Q1
2. 10.1002/cmdc.201200585IF: 3.4 Q2
3. 10.1016/j.ejmech.2015.08.010IF: 5.9 Q1
4. 10.1016/j.jinorgbio.2009.10.011IF: 3.2 Q2
5. 10.1016/j.ejmech.2016.10.020IF: 5.9 Q1
6. 10.1007/s00109-007-0281-3IF: 4.2 Q1
7. 10.1039/d2ob00345gIF: 2.7 Q2